Novavax疫苗向新西兰申请临时批准,Medsafe审查(图)
TVNZ11月4日报道,Novavax公司已申请在新西兰使用其新冠疫苗的临时批准。它宣布其申请已提交给新西兰的医疗监管机构Medsafe。

Novavax公司首席执行官Stanley Erck说:“我们仍然专注于提供我们的疫苗,它建立在一个经过验证的疫苗平台上,并感谢新西兰政府对我们的新冠疫苗项目的持续合作和信任。”
12月,新西兰政府宣布Novavax是其当时获得的两种新冠疫苗中的一种。它已同意购买1072万剂,够536万人使用。
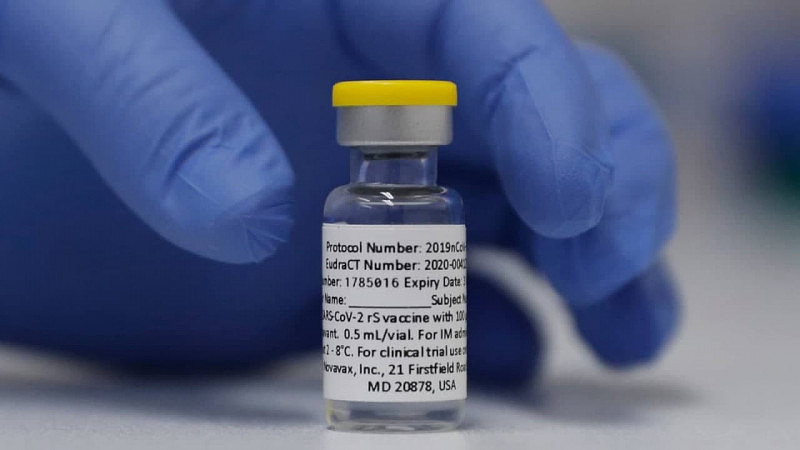
(图片来源:TVNZ)
在Medsafe授予临时批准后,该疫苗仍需由政府部长小组签署,才能在新西兰使用。
Erck说,Novavax公司提交的文件还包括在美国和墨西哥进行的一项3期试验的临床数据,该试验证明了对中度和重度疾病的100%保护,以及90.4%的总体疗效。
在英国进行的一项有1.5万名参与者的试验的临床数据此前已提交给Medsafe。该疫苗对原始毒株的疗效为96.4%,对Alpha毒株的疗效为86.3%,总体疗效为89.7%。
10月14日,卫生主管Caroline McElnay接受了关于Novavax的提问,他说它没有像辉瑞公司的疫苗那样被广泛使用。
“这并不是说对Novavax本身有什么意见,只是说我们在新西兰有辉瑞疫苗。它被广泛使用,它是安全的,我们要求所有新西兰人都接种辉瑞疫苗。"
Novavax还申请在英国、澳洲、加拿大和欧盟使用该疫苗。它预计在今年年底前向美国FDA提交申请。
该公司说,疫苗被包装成即用型液体配方,装在一个小瓶里,一个瓶子有10剂。每剂0.5mL,间隔21天接种。Novavax说,疫苗可以储存在2-8摄氏度的环境中,可以利用现有的疫苗供应和冷链渠道。
根据免疫咨询中心的说法,蛋白质疫苗可能包括从病毒或细菌中提取的片段。它们还可能包括与蛋白质结合的细菌糖/碳水化合物分子。它列举了破伤风、白喉和脑膜炎球菌疫苗。
已与Medsafe公司联系,要求其发表评论。其网站上称已经收到了Novavax的申请。
(Violet)



 +61
+61 +86
+86 +886
+886 +852
+852 +853
+853 +64
+64


